서 론
재료 및 방법
결과 및 고찰
1. 혐기소화액 및 혐기소화액비의 이화학적 성상, 비효성분 분석
2. 혐기소화액 및 혐기소화액비의 중금속 함량, 병원성미생물 분석
3. 시료 형태별 미량영양소 분석 및 부숙도 평가
결 론
서 론
국내 축산산업 성장으로 인해 가축분뇨의 배출량은 지속적으로 늘어날 전망이다 (Kim et al., 2016a). 국내 가축분뇨 발생량은 2020년 기준 연간 5,188만톤에 달하고, 이중 약 87%를 퇴·액비화 로 활용되고 있으며, 나머지는 정화방류 등으로 처리되고 있다 (ME, 2021). 가축분뇨 자원화 방법에는 퇴·액비화 외에도 바이오가스 생산을 통한 에너지화를 들 수 있다. 바이오가스 생산은 가축분뇨의 처리와 동시에 에너지의 획득이라는 장점이 있어서 그 효용가치가 높으며 (Han et al., 2013), 이산화탄소를 증가시키지 않으면서 화석연료를 직접 대체 할 수 있는 농업부문의 주요한 에너지 생산기술이다 (Yoon et al., 2012). 이처럼 혐기성소화는 유기성폐기물을 안전하게 재활용하여 재생에너지인 바이오가스를 생산하는 과정이라 할 수 있다 (Alburquerque et al., 2012).
혐기소화 과정에서 탄소는 메탄가스로 전환되어 회수·이용되지만 질소, 인산, 카리 등과 같은 영양물질이 다량 잔존하는 형태의 소화액을 발생시키므로 이를 처리하기 위한 추가적인 최종처리 방법이 요구된다 (Han et al., 2013). 주로 최종처리에 활용되는 방법으로는 액비화 및 정화처리가 있다. 정화처리의 경우 앞서 언급한바와 같이 소화액 내 영양물질이 다량 잔존하고 있기 때문에 방류수 수질기준에 만족하기 어려울뿐만 아니라 경제적 부담이 가중된다 (Kim et al., 2016b). 이와 같은 이유로 실제 국내 가축분뇨 혐기소화시설 현황 및 운영 실태를 조사한 연구결과에 따르면 혐기소화 후 발생하는 소화액의 처리방법 중 대부분 액비화 방법을 채택하는 것으로 보고하고 있다 (Jeong et al., 2014).
가축분뇨 유래 혐기소화시설은 가축분뇨의 적절한 처리 및 재생에너지 생산을 통한 탄소중립의 기여 할 수 있게 하나, 법률 상 가축분뇨 유래“혐기소화액, 혐기소화액비”에 대한 별도의 정의와 기준이 없어 품질관리가 적절하게 이루어지고 있지 않고 있는 실정이다. 또한 미부숙된 액비가 토양에 투입될 경우 점오염원 또는 비점오염으로 작용하여 수질·대기·토양환경에 악영향을 미칠 수 있음으로 적절한 관리 및 혐기소화액 및 혐기소화액비의 이용을 위해서는 물리·화학적 특성을 파악하는 것이 무엇보다 중요하다 (Kim et al., 2005).
본 연구에서는 바이오가스 시설에서 생산되는 혐기소화액과 혐기소화액비를 「비료 공정규격설정 및 지정」 상 “가축분뇨발효액”기준을 근거로 비효성분의 조성, 이화학적 성상, 병원미생물, 중금속 함량, 부숙도등을 조사·평가함으로서, 혐기소화액 및 혐기소화액비에 대한 품질특성을 도출하였다.
재료 및 방법
국내에서는 아직 호기적으로 2차 처리된 혐기소화액에 대한 정의가 없기 때문에 본 연구에 한하여 혐기소화 후 발생하는 액을 혐기소화액, 혐기소화액을 호기적 처리한 액상물을 혐기소화액비라고 정의하였다. 본 연구에서는 국내 바이오가스시설에서 생산되는 혐기소화액 및 혐기소화액비 품질 특성을 조사하기 위하여 2021년 6월~7월 동안 5개소의 혐기소화액 5점 및 혐기소화액비 5점의 샘플을 수집하였으며, 각 바이오가스 플랜트의 유입원료의 종류 및 비율을 Table 1에 나타냈다. 한편, 가축분뇨 자원화시설 표준설계도에 따르면 돼지분뇨 (BOD 33,000 mg/L 기준)의 호기성 액비화 시 HRT (Hydraulic Retention Time)는 0.03 ㎥-air/min·㎥ 조건에서 45일 정도의 시간의 소요되는데 (ME, 2023), 본 연구에서 수집된 혐기소화액비는 모두 30일 이상 폭기처리가 된 것을 수집하였다.
Table 1.
The current status of biogasification facilities to be investigated.
수집된 혐기소화액 및 혐기소화액비 샘플은 비료공정규격설정 기준 항목에 따라 질소 (N), 인산 (P2O5), 가리 (K2O), 비소 (As), 카드뮴 (Cd), 수은 (Hg), 납 (Pb), 크롬 (Cr), 구리 (Cu), 아연 (Zn), 니켈 (Ni), 염분 (NaCl), 수분함량 (Moisture content)과 병원성미생물인 E. coli(0157:H7), salmonella spp.을 분석하였다. 또한 그 외로 수소이온농도 (pH), 전기전도도 (EC), 화학적산소요구량 (CODCr), 용해성화학적산소요구량 (SCODCr), 암모니아성질소 (NH4-N), 질산성질소 (NO3-N), 석회 (CaO), 마그네슘 (MgO), 붕소 (B2O3), 망간 (MnO), 철 (Fe), 몰리브덴 (Mo), 발아지수 (Germination index, GI), 부숙도 (Maturity)를 분석하여 혐기소화액 및 혐기소화액비 샘플의 종합적인 품질을 평가하였다.
T-N, NH4-N, NO3-N은 각각 황산법, 증류법, 데바루다합금법으로 측정하였다. P2O5, K2O, As, Cd, Pb, Cr, Cu, Ni, Zn, Ca, Mg, Fe, Mo, Mn, B는 마이크로웨이브 (QWave1000, Questron Technologies, USA)로 산 가수분해 후 ICP (Spectro Blue, SPECTRO Analitical Instruments, Germany)로 각각 측정하였으며, Hg는 마이크로웨이브 (QWave1000, Questron Technologies, USA)로 산 가수분해 후 수은분석기 (RA-5, NIC, Japan)를 이용하여 측정하였다. 염분 농도는 ICP (Spectro Blue, SPECTRO Analitical Instruments, Germany)로 Na로 정량한 후 환산인자를 통해 NaCl로 환산하여 계산하였고, 병원성미생물인 E. coli(0157:H7), salmonella spp.은 미생물 시험법으로 분석하였다. 부숙도는 암모니아와 색도을 이용한 기계적 부숙도 측정 방법 (LMQ2000, KSP, Korea)과 종자발아법을 이용한 발아지수 (GI)를 측정하였다. 그 외 pH와 EC는 각각 수질다항목측정기 (HANNA Hi-8424N)를 이용하여 측정하였으며, 수분함량 및 화학적산소요구량은 공정시험기준법에 따라 분석하였다.
결과 및 고찰
1. 혐기소화액 및 혐기소화액비의 이화학적 성상, 비효성분 분석
(1) pH, 수분의 함량 및 총 고형물 함량
본 연구에서 조사된 혐기소화액 및 혐기소화액비의 pH, 수분 함량, 총 고형물 함량의 분석 결과는 Table 2에 나타냈다. 혐기소화액 및 혐기소화액비에 대한 pH의 평균값은 각각 8.21, 8.69이었으며, 수분함량은 각각 96.99%, 97.46%, 총 고형물의 함량 각각 3.01%, 2.54%로 측정되었다. Kim et al. (2015)에 따르면 일반적으로 돈분뇨 액비화의 경우 부숙이 진행됨에 따라 pH는 증가하는 것으로 알려져 있다. 혐기소화액비의 pH는 혐기소화액비 보다 pH가 높게 측정되었고, 그 외 수분함량의 경우 혐기소화액, 혐기소화액비 모두 거의 비슷한 특성을 나타냈다.
Table 2.
pH and moisture properties of AD and ADLF0
| pH | MC3 | TS4 | ||
| (%) | (%) | |||
| AD1 (n=5) | Mean | 8.21 | 96.99 | 3.01 |
| Min4 | 8.00 | 96.26 | 1.58 | |
| Max5 | 8.45 | 98.42 | 3.74 | |
| Standard deviation | 0.16 | 0.79 | 0.79 | |
| ADLF2 (n=5) | Mean | 8.69 | 97.46 | 2.54 |
| Min5 | 6.46 | 96.75 | 1.16 | |
| Max6 | 9.48 | 98.34 | 3.25 | |
| Standard deviation | 1.25 | 0.61 | 0.61 | |
| Official standard of commercial fertilizer | - | ≥95 | - | |
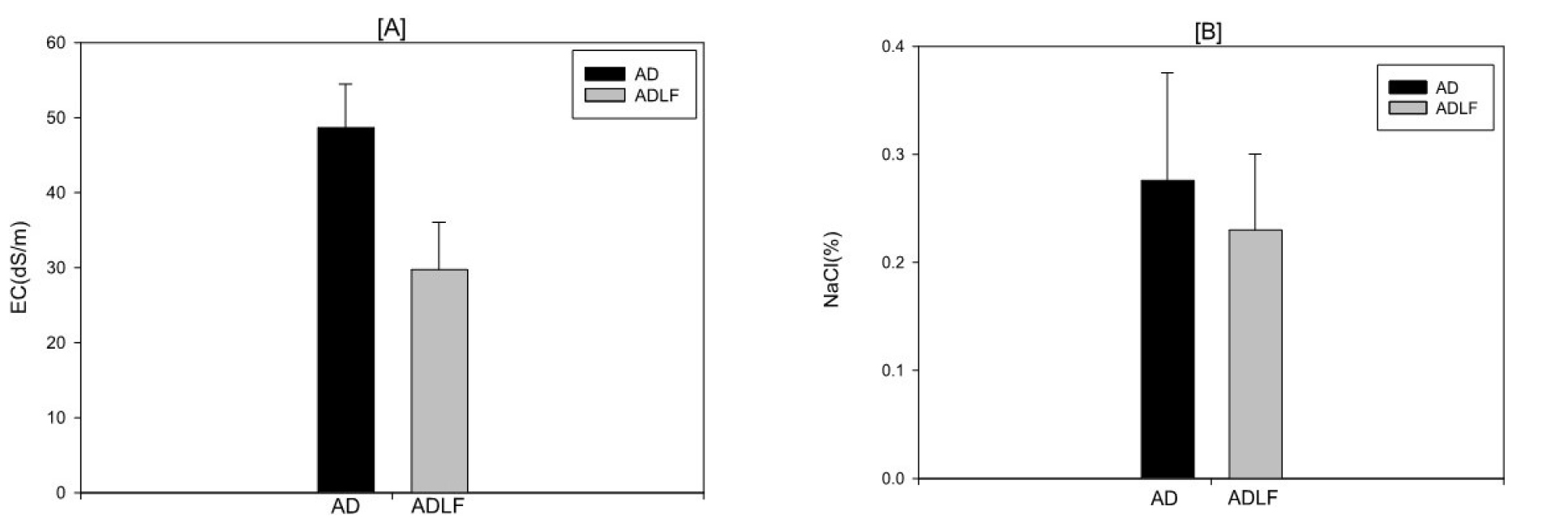
(2) EC, NaCl의 함량
혐기소화액 및 혐기소화액비의 EC, NaCl의 분석 결과는 Figure 1에 나타냈다. 혐기소화액의 이화학성상 평균값은 EC 48.68 dS/m, NaCl 0.28%로 나타났으며, 혐기소화액비는 EC 29.74 dS/m, NaCl 0.23%로 분석되었다. Kim et al. (2004) 연구에 따르면 돈분 slurry 저장 액비 (n=70)의 경우 EC의 평균치는 34 mS/cm로 나타났는데, 본 연구에서 혐기소화액의 EC 경우 돈분 slurry 액비 보다 높은 것으로 나타났다. 또한 혐기소화액을 액비화 처리한 혐기소화액비의 경우 혐기소화액 샘플 대비 낮아지는 경향을 보였으며, 이와 유사하게 Byeon et al. (2020) 연구에서도 혐기소화액 액비화 처리 전보다 부숙이 됨에 따라 전기전도도가 감소하는 경향으로 보고되었다. Ca, Mg, Na, SO42-, Cl 등의 특정한 양분의 집적은 삼투압작용에 의해 작물의 토양수 이용률을 저하시키고, 이온독성 발현과 타 유효이온의 흡수를 저해하여 작물의 생육장해를 유발시킨다 (Oh et al., 2010). 일반적으로 혐기소화액의 경우 난분해성 유기물 함량과 염류조성이 여타 부산물과 차이가 있기 때문에 혐기소화액비의 EC 값은 토양 환원 시 시용량 결정 및 부숙도 평가에 있어 중요한 요인이 될 수 있다. 그러므로 안정적인 농지 환원을 위해서는 EC를 중심으로 한 살포 프로그램이 필요하다 (Hong et al., 2012). 또한 염분이 많은 소화액을 토양에 과도하게 투여하거나 계속 시비할 경우 토양의 염분도가 증가하여 식물 생장을 저해 할 수 있다 (Alburquerque et al., 2012). 본 연구결과 혐기소화액 및 혐기소화액비의 일부 샘플에서 비료공정규격 기준에 염분함량이 부합하지 못하였다.
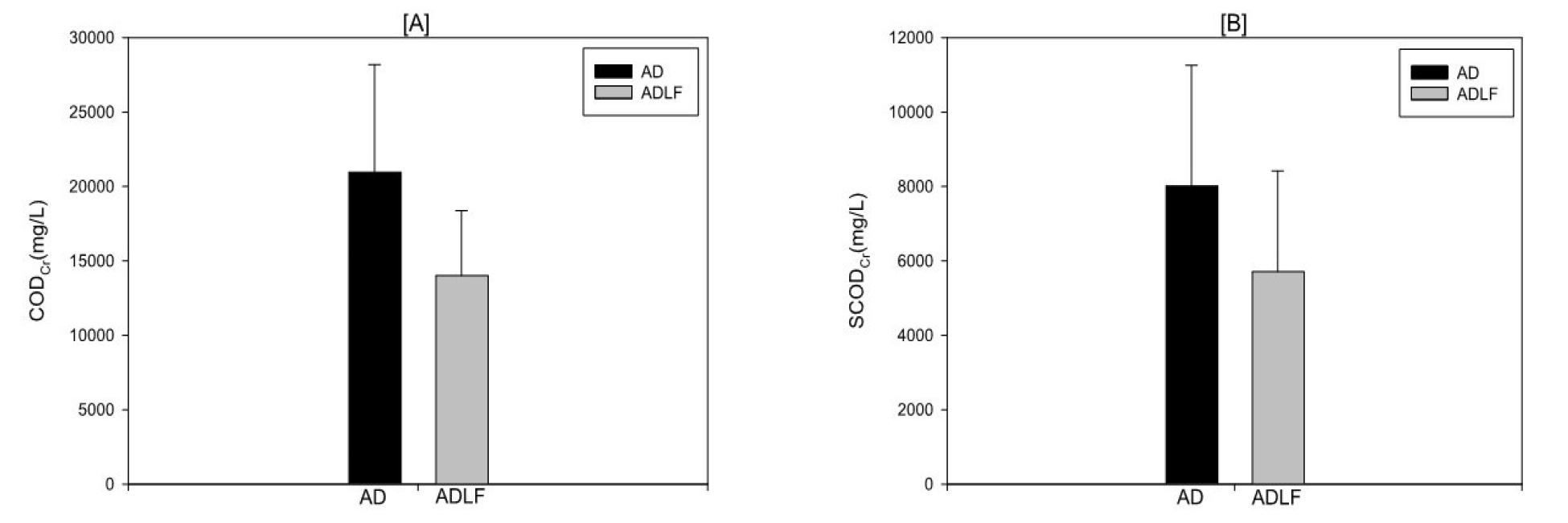
(3) CODCr, SCODCr의 함량
혐기소화액 및 혐기소화액비의 CODCr, SCODCr의 함량은 Figure 2와 같다. 혐기소화액의 이화학성상 평균값은 CODCr 20,973 mg/L, SCODCr 8,016 mg/L로 나타났으며, 혐기소화액비는 CODCr 14,022 mg/L, SCODCr 5,710 mg/L로 나타났다. COD는 BOD와 더불어 오염물질 정도의 지표로 이용되고 있는데, COD의 경우 Jung et al. (2015) 연구에 따르면 액비화 시 전처리로서 고액분리만으로 상당량을 제거할 수 있다고 보고 하였다. 또한 다수의 유사 연구에서 보고된 ‘부숙액비’의 COD 농도의 경우 본 연구의 혐기소화액 대비 상대적으로 낮은 농도로 분포하였는데 (Kang et al., 2017), 이를 고려했을 때 혐기소화액의 총 고형물에서 유래하는 BOD나 COD 등을 전처리 단계에서 최대한 제거하는 것이 바람직하다고 사료된다. 본 연구에서는 혐기소화액 대비 혐기소화액비의 제거율은 평균적으로 약 CODcr 33.14%, SCODcr 28.77% 나타냈다.
(4) T-N, P2O5, K2O의 함량 및 각 성분의 합계량
혐기소화액 및 혐기소화액비의 T-N, P2O5, K2O 및 NPK 합계량 (T-N+P2O5+K2O)은 Table 3과 같다. 혐기소화액의 비료성분 평균값은 T-N 0.53%, P2O5 0.13%, K2O 0.30% 및 NPK합계량은 0.95%로 나타났으며, 혐기소화액비는 T-N 0.30%, P2O5 0.08%, K2O 0.27% 및 NPK합계량은 0.65%로 나타났다. 혐기소화액비의 T-N 함량 농도는 혐기소화액 대비 23% 감소하였고, P2O5, K2O의 함량은 혐기소화액 대비 각각 0.05%,0.03%로 감소하였다. 비료공정규격 기준인 T-N+P2O5+K2O의 성분합계량 0.3% 이상에 대해서 혐기소화액 0.95% 및 혐기소화액비 0.65%로 각각 비료공정규격의 기준에 부합하였다.
Table 3.
N, P2O5, and K2O properties of AD and ADLF.
| N | P2O5 | K2O | N+P2O5+K2O | ||
| (%) | |||||
| AD1 (n=5) | Mean | 0.53 | 0.13 | 0.30 | 0.95 |
| Min3 | 0.46 | 0.04 | 0.24 | 0.85 | |
| Max4 | 0.60 | 0.21 | 0.33 | 1.07 | |
| Standard deviation | 0.06 | 0.07 | 0.03 | 0.09 | |
| ADLF2 (n=5) | Mean | 0.30 | 0.08 | 0.27 | 0.65 |
| Min3 | 0.21 | 0.01 | 0.13 | 0.39 | |
| Max4 | 0.45 | 0.16 | 0.35 | 0.89 | |
| Standard deviation | 0.08 | 0.06 | 0.08 | 0.16 | |
| Official standard of commercial fertilizer | - | - | - | ≥0.3 | |
(5) NH4-N, NO3-N의 함량
혐기소화액 및 혐기소화액비의 NH4-N, NO3–N의 함량은 Table 4과 같다. 혐기소화액의 NH4-N, NO3–N 평균값은 각각 3,911 mg/L, 228 mg/L로 나타났으며, 혐기소화액비의 NH4-N, NO3–N 평균값은 각각 1,923 mg/L, 334 mg/L로 나타났다. 모든 식물생장에 꼭 필요한 요소로 대표적으로 N (질소), P (인산), K (카리) 등이 있으며 (Yang, 2008), 이 중 식물의 생장에 큰 영향을 주는 N에 대한 형태가 매우 중요하다. 질소의 수중 형태는 암모니아성 질소, 아질산성 질소, 질산성 질소의 상태로 존재한다 (Lee et al., 2008). 액비가 토양에 스며들어 뿌리로 흡수하는 형태는 질산성 질소이며, 암모니아 형태도 흡수를 하지만, 흡수시간이 오래 걸려 뿌리로 흡수되기 전에 토양으로 유출되는 양이 더 많다. 따라서 식물생장을 위해서는 액비 중에 질산성 질소의 형태의 N 함유량이 높아야 한다 (Paik et al., 2017). Jeon et al. (2012)과 Kang et al. (2017)이 보고한 부숙액비와 본 연구에서 분석된 혐기소화액과 비교 시 NH4-N의 농도 (3,911 mg/L)는 매우 높았으며, NO3-N 농도 (228 mg/L)는 상대적으로 낮았다. 혐기소화액비의 경우 NH4-N의 농도 (1,923 mg/L)는 높았으며, NO3-N 농도 (334 mg/L) 는 상대적으로 낮았다.
Table 4.
NH4-N and NO3-N properties of AD and ADLF.
| NH4-N | NO3-N | ||
| (mg/kg) | |||
| AD1 (n=5) | Mean | 3,911 | 228 |
| Min3 | 3,098 | 116 | |
| Max4 | 4,500 | 348 | |
| Standard deviation | 525 | 86 | |
| ADLF2 (n=5) | Mean | 1,923 | 334 |
| Min3 | 489 | 108 | |
| Max4 | 2,969 | 804 | |
| Standard deviation | 835 | 225 | |
2. 혐기소화액 및 혐기소화액비의 중금속 함량, 병원성미생물 분석
비료공정규격에서는 가축분뇨발효액 내 중금속의 허용 가능 최대량을 As 5 mg/kg, Cd 0.5 mg/kg, Hg 0.2 mg/kg, Pb 15 mg/kg, Cr 30mg/kg, Cu 50 mg/kg, Ni 5 mg/kg, Zn 130mg/kg로 규정하고 있고, 또한 병원성미생물인 E. Coil(O157:H7)와 Salmonella spp.도 검출되지 않아야 한다.
중금속 8종 (As, Cd, Hg, Pb, Cr, Cu, Ni and Zn)의 특성으로는 중금속 8종이 포함된 미량원소를 성장촉진, 사료의 효율 개선 등의 목적으로 사료에 첨가되는데, 동물체 내에서 전량흡수 되지 않고, 일부 분뇨로 배출되어 액비 의 시비 시 토양 내 중금속 축적 및 지하수 및 지표수를 오염시킨다 (Ahn et al., 2021). 병원성미생물의 경우 가축분뇨 발효액을 토양에 사용하여 식물을 통해 사람에게 전염될 수 있는 위험요소 중에 하나이다 (Jeon et al., 2013).
혐기소화액 및 혐기소화액비의 As, Cd, Hg, Pb. Cr, Cu, Zn, Ni은 Table 5과 같다. 혐기소화액의 중금속 평균값은 Pb 0.49 mg/kg, Cr 0.89 mg/kg, Cu 13.90 mg/kg, Zn 58.21 mg/kg, Ni 0.47 mg/kg로 나타났으며, 혐기소화액비는 Pb 0.23 mg/kg, Cr 0.76 mg/kg, Cu 9.80 mg/kg, Zn 51.78 mg/kg, Ni 0.41 mg/kg로 나타났다. As, Cd, Hg는 혐기소화액 및 혐기소화액비 모두 불검출로 나타났다. 그 외 혐기소화액 및 혐기소화액비의 모든 샘플에서는 병원성미생물인 E. Coil(O157:H7), Salmonella spp.은 검출되지 않았다.
Table 5.
Characteristics of heavy metals contents and detection of pathogenic bacteria in AD and ADLF.
| As | Cd | Hg | Pb | Cr | Cu | Ni | Zn | E. Coil (O157:H7) | Salmonella spp. | ||
| (mg/kg) | |||||||||||
| AD1 (n=5) | Mean | N.D.5 | N.D. | N.D. | 0.49 | 0.89 | 13.90 | 0.47 | 58.21 | N.D. | N.D. |
| Min3 | - | - | - | N.D. | 0.34 | 10.75 | 0.36 | 39.89 | - | - | |
| Max4 | - | - | - | 1.23 | 1.62 | 18.04 | 0.58 | 91.31 | - | - | |
| Standard deviation | - | - | - | 0.67 | 0.49 | 2.97 | 0.10 | 19.45 | - | - | |
| ADLF2 (n=5) | Mean | N.D. | N.D. | N.D. | 0.23 | 0.76 | 9.79 | 0.41 | 51.78 | N.D. | N.D. |
| Min3 | - | - | - | N.D. | 0.26 | 4.75 | 0.3 | 21.53 | - | - | |
| Max4 | - | - | - | 1.14 | 1.77 | 14.19 | 0.56 | 77.54 | - | - | |
| Standard deviation | - | - | - | 0.51 | 0.66 | 3.76 | 0.10 | 23.76 | - | - | |
|
Official standard of commercial fertilizer | ≤ 5 | ≤ 0.5 | ≤ 0.2 | ≤ 15 | ≤ 30 | ≤ 50 | ≤ 5 | ≤ 130 | N.D. | ||
3. 시료 형태별 미량영양소 분석 및 부숙도 평가
혐기소화액의 미량영양소 평균값은 CaO 1,219.41 mg/kg, MgO 429.11 mg/kg, B2O3 65.65 mg/kg, MnO 11.18 mg/kg, Fe 255.41 mg/kg, Mo 8.56 mg/kg으로 나타났다. 혐기소화액비의 경우 CaO 693.73 mg/kg, MgO 268.18 mg/kg, B2O3 56.76 mg/kg, MnO 6.63 mg/kg, Fe 190.70 mg/kg, Mo 7.30 mg/kg로 나타났다 (Table 6).
Table 6.
Micronutrients contents properties of AD and ADLF.
| CaO | MgO | MnO | B2O3 | Fe | Mo | ||
| (mg/kg) | |||||||
| AD1 (n=5) | Mean | 1,219.41 | 429.11 | 11.18 | 65.64 | 255.41 | 8.56 |
| Min3 | 392.46 | 68.71 | N.D. | 50.59 | 54.88 | 6.84 | |
| Max4 | 1,899.88 | 806.95 | 24.15 | 87.87 | 379.81 | 12.48 | |
| Standard deviation | 596.83 | 277.54 | 8.18 | 12.34 | 122.51 | 2.06 | |
| ADLF2 (n=5) | Mean | 693.73 | 268.18 | 6.63 | 56.76 | 190.70 | 7.30 |
| Min3 | 184.60 | N.D. | N.D. | 44.18 | 54.07 | 6.03 | |
| Max4 | 1,250.73 | 791.09 | 16.33 | 66.62 | 387.65 | 8.59 | |
| Standard deviation | 383.22 | 296.75 | 6.15 | 7.75 | 121.63 | 0.90 | |
부숙도란 액비의 경작지 시용 적정성 여부 (Jeong et al., 2022)를 점검할 수 있는 지표로서 법령에 나와있는 정의로는 퇴비·액비의 원료가 퇴비·액비화 과정을 거치어 식물과 토양에 대해 안정적인 반응을 나타타는 것으로 정의하고 있다. 본 연구에서는 기계적부숙도측정 및 발아지수를 이용하여 혐기소화액과 혐기소화액비의 부숙도를 평가하였으며, 그 결과 기계적부숙도측정은 혐기소화액 및 혐기소화액비 총 10점 중 1점만 부숙으로 나타났으며, 중숙 3점, 미숙 6점으로 나타났다. 또한 종자발아법을 이용한 발아지수 (GI)의 경우 부숙 판정을 받은 샘플에서도 모두 GI 0으로 나타났는데 (Table 7), 이는 상대적으로 높은 염분농도 (또는 EC)와 가스장애를 나타내어 발아 및 초기 성장을 둔화시킬 수 있는 NH4-N의 높은 농도에 기인된 것으로 사료된다.
결 론
본 연구에서는 가축분뇨와 음식물폐수 혼합 처리하는 에너지화 (바이오가스) 시설에서 생산된 혐기소화액 및 혐기소화액비 형태별 품질 특성을 파악하고자 5개소를 대상으로 혐기소화액 (n=5) 및 혐기소화액비 (n=5)를 수집하여 비효성분의 조성, 이화학적 성상, 병원성미생물, 중금속 함량, 부숙도 등을 분석하였다.
Jeon et al. (2012)와 Kang et al. (2017)가 보고한 돼지분뇨 부숙액비의 이화학적 성상과 비교하였을 때, 본 연구의 혐기소화액 및 혐기소화액비의 EC값과 NH4-N은 비교적 높은 농도로 분포하는 특징을 나타냈다. 혐기소화액 및 혐기소화액비의 높은 EC값은 투입 원료인 음폐수의 염분농도에서 기인된 것으로 사료되며, NH4-N의 경우는 혐기소화액의 특성상 C/N비의 불균형 등으로 인하여 호기적 조건에서도 질산화가 원활히 이루어지지 않았기 때문인 것으로 사료된다. 한편, 혐기성 공정을 통해 생산된 모든 혐기소화액 샘플에서 NO3-N의 농도 (116~348 mg/L)가 측정된 것은 본 연구에서 해석하지 못한 한계점이다. 따라서 향후 바이오가스플랜트에서의 가축분뇨와 음폐수 혼합 유입 특성에 따른 혐기소화액의 EC 상관성과 NO3-N의 기작 특성 및 혐기소화액의 액비화 시 단위공정별 인자 (C/N비, 공기공급량, HRT 등)에 따른 물질변화 특성을 세부적으로 조사할 필요가 있다.
본 연구의 혐기소화액과 혐기소화액비의 품질은 비료공정규격 기준에 대부분이 만족하는 것으로 평가되었으나, 기계적 부숙도는 대부분의 샘플에서 미숙 또는 중숙으로 판정되었고, 종자발아법에서의 발아지수는 0으로 평가되었다.
또한 염류물질 등을 간접적으로 평가하는 EC의 경우 조사된 혐기소화액비의 경우 평균 29.74 mS/cm로서 일반적인 가축분뇨 부숙액비 (EC 8~15 mS/cm 수준)에 비해 상대적으로 높은 농도로 분포되었다. 액비 (혐기소화액, 혐기소화액비)의 품질규격이나 부숙도 평기기준이 미비하여 저품질 액비 생산에 따른 경종농가의 시용이 기피되고 있는 실정이다. 그러므로 이에 대한 대안으로서 액비 (혐기소화액, 혐기소화액비)의 품질 규격을 명확하게 확립하는 것이 중요할 것으로 판단되고, 또한 부숙도에 직·간접적으로 영향을 미치는 염류물질과 암모니아성질소 등을 혐기소화액의 액비화 시작 전 단계에서 최대한 감소시킬 필요가 있을것으로 사료된다. 이에 대한 품질 개선 방향성은 추가적인 연구가 필요할 것으로 판단된다.